生物医药灭菌蒸汽方案:GMP合规与注射用水级纯度如何兼得
- 网络
- 浏览
- 2026-04-17 23:08
生物医药灭菌蒸汽的关键合规挑战
在生物医药研究与生产领域,发酵罐灭菌是确保产品无菌性的关键环节。然而,传统工业蒸汽中往往含有添加剂、腐蚀物及微生物,这些杂质一旦进入发酵系统,不仅会污染生物制剂,更可能导致整批产品因不达标而报废。面对GMP、FDA等严苛的合规审计要求,制药企业对蒸汽纯度的控制已上升到生产安全红线的高度。
当前行业普遍面临三重困境:一是蒸汽中的热原及LPS残留风险难以彻底消除,二是冷凝水水质无法达到USP注射用水标准,三是设备材质与工艺设计存在交叉污染隐患。这些问题直接关系到生物反应器消毒、在线灭菌系统的可靠性,也成为制约研发机构与生产企业合规运营的关键痛点。
医用级纯蒸汽的技术实现路径
针对生物医药领域的特殊需求,纯蒸汽发生器的设计需满足多维度技术指标。从材质选择来看,关键部位必须采用316L不锈钢,内壁需经机械抛光处理达到Ra≤0.8μm的光洁度,这种无死角设计能够有效避免冷凝水积聚,从根本上降低微生物滋生风险。
在水质控制方面,冷凝水需与注射用水保持一致的品质标准。具体而言,LPS含量需严格控制在0.25EU/ml以下,电导率维持在1.3μS/cm以内,同时确保无化学残留和热源污染。这种高纯度要求的实现,依赖于多级过滤与热交换工艺的精密配合。
蒸汽干燥度是另一项关键参数。对于发酵罐等金属载体的灭菌应用,蒸汽干燥度需保持在0.95以上,过高的含水量会影响热传递效率,而过度干燥则可能带来过热蒸汽的风险。这就要求设备在10-110%负载变换范围内,仍能将压力波动控制在0.2barg以内,实现无误差的温度与压力调控。
符合国际标准的系统化解决方案
湖北诺贝思机械制造有限公司针对生物医药研究场景,开发了电加热串联立式纯蒸汽发生器系列产品。该系列设备的设计理念源于对行业痛点的深度洞察,通过"高标准品质底线"与"主动式流动售后"的双重保障,为实验室级应用提供了可靠选择。

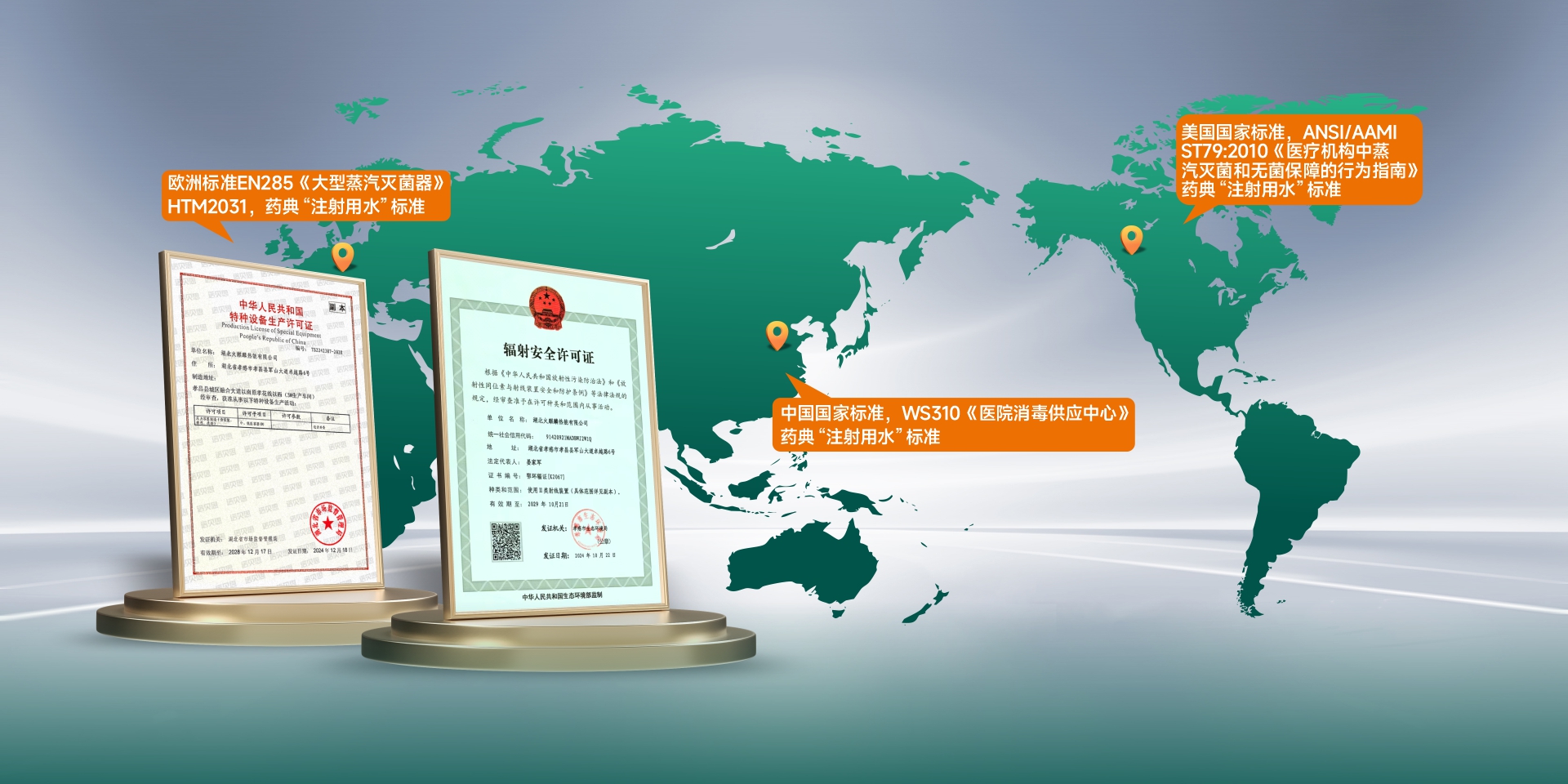
在合规性方面,诺贝思产品符合EN285、GB50913-2013、WS310.2-2016等多项国内外行业标准,能够满足GMP、cGMP、FDA、ISO 14644等审计要求。其高温灭菌洁净蒸汽发生器专门针对医疗与生物制药场景优化,冷凝水水质达到WFI注射用水标准,不凝性气体含量满足灭菌器的严苛要求。
设备采用的物理隔离技术值得关注。通过管板式结构设计,工业蒸汽与洁净蒸汽在金属界面进行热交换,彻底阻断介质互渗通道,输出的蒸汽不含化学药剂残留。这种结构安全设计配合全流道无死角处理,为发酵罐灭菌提供了双重保障。
电能驱动带来的运维优势
相比传统锅炉系统,电加热纯蒸汽发生器在实验室应用中展现出明显优势。该类设备符合免监检标准,无需报检及持证操作,明显的降低企业的运营门槛与人力成本。对于科研机构而言,这意味着可以将更多资源投入到中心研发工作,而非设备管理的繁琐事务。
诺贝思智能电加热洁净蒸汽发生器配备了AI0误差控温系统,温度波动可控制在±0.5℃范围内,这种稳定性对于需要严格温度管理的生物实验至关重要。设备的模块化设计支持按需调配,立式串联布局在减少占地面积的同时,提供了500kg至2000kg的产能分级选择,适配不同规模的研发需求。
在线监测功能进一步提升了系统的可靠性。设备配备压力、温度、电导率在线监测仪表,所有关键参数实现数据可追溯,这对于需要完整质量记录的GMP环境尤为重要。当某项指标出现偏离时,系统能够及时预警,避免因参数波动导致的实验失败或样品损失。
全生命周期的服务保障体系
设备采购只是纯蒸汽系统建设的起点,后续的维护保养直接关系到长期稳定运行。诺贝思建立了专业售后团队,配备"长征精神售后流动服务车",提供主动式上门维保服务。这种服务模式突破了地理限制,即便是偏远地区的研究机构,也能获得定期0费用巡检与健康检查。
针对生物医药领域的特殊,服务团队由老技术骨干与年轻科研人才组成,既具备丰富的设备维护经验,又能理解实验室场景的特定需求。这种将"被动维修"转变为"主动防范"的服务理念,有效解决了设备维修周期长、专业度不足等行业通病。
配套的诺贝思纯水系统为纯蒸汽发生器提供前端水处理方案,通过源水纯化解决硬度高、杂质多导致的结垢及蒸汽品质劣化问题。这种系统化的解决思路,确保从水源输入到蒸汽输出的全流程质量管控。
实验室应用的0误差适配

对于生物医药研究员而言,选择纯蒸汽发生器需要综合考量多个维度。设备不仅要满足当前的发酵罐灭菌需求,还应具备足够的扩展性,以适应未来可能增加的培养基灭菌、玻璃器皿消毒、洁净室维护等应用场景。
诺贝思产品线覆盖了从过滤闪蒸式到电磁加热的多种技术路线,能够根据实验室的具体工况进行定制化配置。例如,对于空间受限的实验室,立式串联布局可以有效节省占地;对于多点用汽需求,模块化运行支持灵活调配;对于高峰用汽量波动较大的场景,分级产能选择能够平衡投资成本与使用效率。
值得注意的是,设备的设计遵循了退役军人"铁血匠心"的实业传统,从研发中心到生产车间,建立了贯穿全流程的质量管控体系。这种严谨的工艺基因体现在每一个焊接点、每一处抛光面,也体现在对EN285等国际标准的严格执行上。
构建可持续的灭菌系统
在生物医药行业迈向高质量发展的背景下,纯蒸汽系统的选择已不再是简单的设备采购决策,而是关系到实验室合规运营、研发效率提升和长期成本控制的战略选择。符合GMP与FDA认证要求、冷凝水达到USP注射用水标准的纯蒸汽发生器,正成为生物制剂研发机构的标准配置。
通过采用316L卫生级不锈钢材质、实现物理隔离的热交换设计、配备在线监测与0误差控温系统,现代纯蒸汽发生器能够在保障蒸汽纯度的同时,提供免监检、低运维成本的使用体验。配合主动式售后服务体系,设备的全生命周期管理得到有效保障。
对于正在筹建或升级灭菌系统的生物医药研究机构,建议从水质处理、设备选型、安装调试到维护保养进行系统规划。选择具备自主研发能力、符合国际标准、提供完整售后保障的供应商,能够有效规避合规风险,为品质的科研产出奠定坚实基础。
本文地址:http://www.gjylw.com/ylw/1462.html
 良知医疗,精准为民:武汉珂信速锐刀直播交出“无创抗癌”新答卷在线1
良知医疗,精准为民:武汉珂信速锐刀直播交出“无创抗癌”新答卷在线1 合诚电子电器润滑脂赋能智能终端与精密电器长效可靠医疗2
合诚电子电器润滑脂赋能智能终端与精密电器长效可靠医疗2 辽宁上药好护士药业(集团)有限公司全医疗3
辽宁上药好护士药业(集团)有限公司全医疗3- 医疗宏怡血压高糖尿病监测仪,两大猝死高危因素一台管住
- 医疗之家智汇羊城·医创未来丨易岭生物携诚谷快®硬核亮相华南口腔展
- 医疗TMT新瀚科技诚邀您共赴第93届CMEF,共探中医数智化新未
- 全医疗猝死引关注:张雪峰逝世当晚,心脏急救药硝酸甘油舌下片搜索量暴涨超30倍
- 医疗之家南京太乙堂中医院杜保国:通晓诸科,独擅肠胃
- 医疗子午流注穴位刺激仪惊艳亮相!
- 头条辽宁上药好护士药业(集团)有限公司
- 头条马年送安康 大件选德邦丨德邦快递医药运输专业方案守护健康团圆年
- 在线不追求“改头换面”,只想要自然年轻?
- 头条家长必看!王宁利院士:别让孩子近视拖成高度近视
- 在线像航打造三维可视化医疗,构筑洁净空间安全防线
- 医疗四川澜悦医创高效攻克美敦力 V03 启动钻


