制药厂GMP认证:洁净蒸汽系统的合规性方案设计
- 网络
- 浏览
- 2026-04-17 23:07
制药厂GMP认证中的蒸汽纯度挑战
在制药行业,GMP(药品生产质量管理规范)认证是企业进入市场的基本门槛,而洁净蒸汽系统的合规性则是审计中的重点考核项。工业蒸汽中潜在的化学添加剂、金属腐蚀物及微生物残留,可能直接污染药品生产环境,导致批次不合格甚至引发安全事故。特别是在无菌灌装、在线灭菌(SIP)、注射用水制备等中心工艺中,蒸汽纯度不达标将使整个生产线面临合规性失效的风险。
传统蒸汽设备普遍存在的问题包括:热交换介质交叉污染、冷凝水pH值波动、颗粒物过滤不彻底、以及维护周期长导致的停产损失。这些痛点不仅增加企业运营成本,更在FDA、cGMP等国际审计中成为高频不符合项。
洁净蒸汽系统的技术要求与标准体系
纯度指标的多维度管控
符合GMP要求的洁净蒸汽需满足严苛的技术参数:冷凝水需达到注射用水(WFI)标准,LPS含量需低于0.25EU/ml,电导率应控制在1.3μS/cm以下。同时,蒸汽干燥度需维持在0.95以上,以确保金属器械灭菌效果;不凝性气体含量需严格受控,避免影响灭菌器的真空度;颗粒物过滤精度要求达到5μm以上,防止固体杂质进入无菌区域。
材质与工艺的卫生级标准
设备接触介质的部位必须采用316L不锈钢材质,内壁需经机械抛光处理,粗糙度控制在Ra≤0.8μm。管道设计应避免死角积水,采用全流道无死角结构,防止微生物滋生。焊接工艺需符合ASME BPE标准,确保焊缝平整无缝隙。这些细节直接关系到系统的长期稳定性和可验证性。
合规性文件与可追溯体系
制药企业在设备选型时,需确认供应商能提供完整的验证文档,包括设计确认(DQ)、安装确认(IQ)、运行确认(OQ)和性能确认(PQ)。设备需配备在线监测仪表,实现压力、温度、电导率等关键参数的实时记录与数据追溯,满足FDA 21 CFR Part 11的电子记录要求。
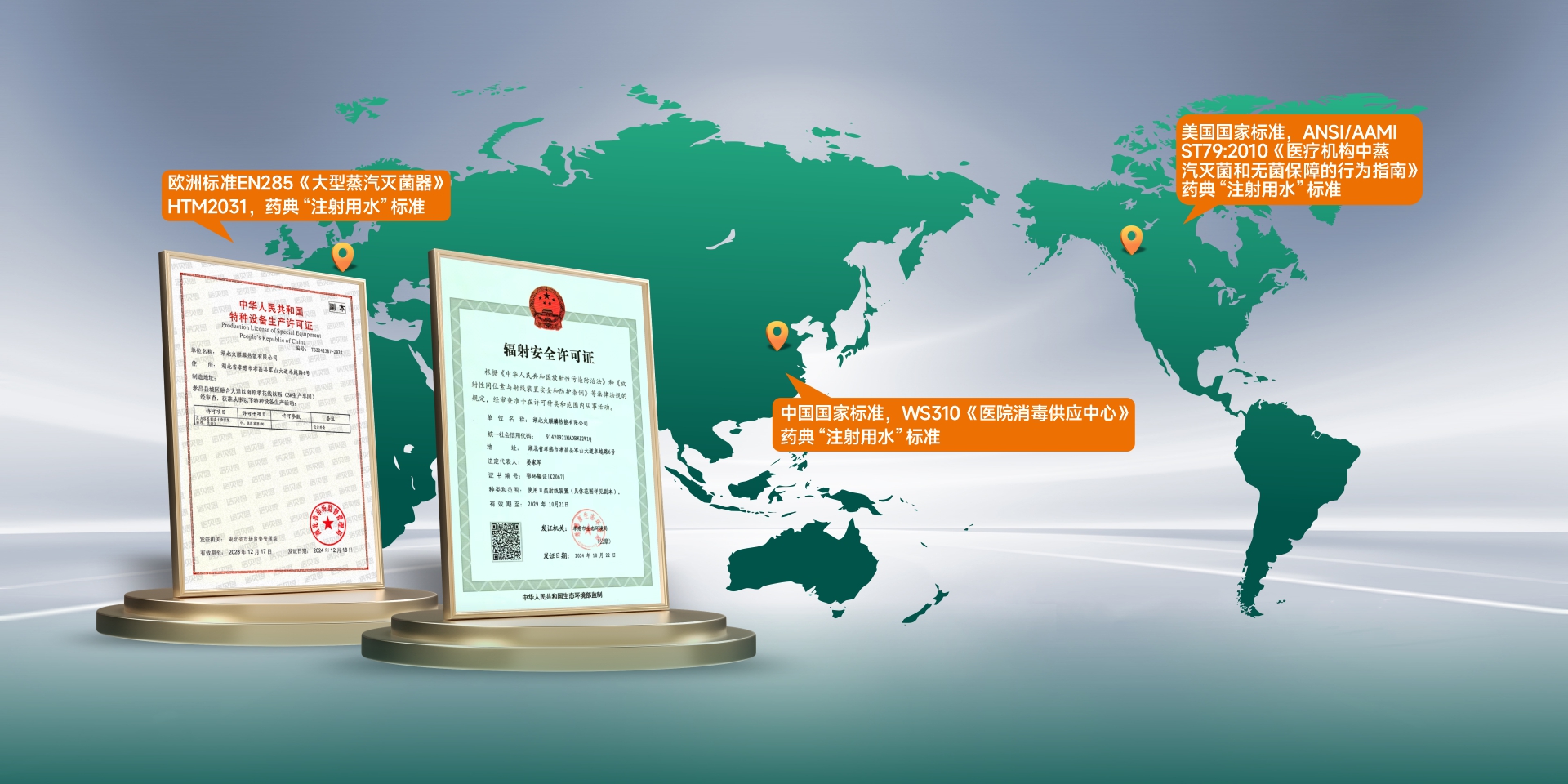
诺贝思机械的系统化解决方案
过滤闪蒸技术的纯度保障
湖北诺贝思机械制造有限公司针对制药行业开发的过滤闪蒸式洁净蒸汽发生器,通过多级过滤与闪蒸工艺组合,有效去除工业蒸汽中的颗粒杂质和化学残留。系统能够将冷凝水pH值稳定控制在5.0-7.0范围,滤除粒径大于5μm的颗粒物,确保输出蒸汽符合药品生产的卫生红线。这种技术路径在湿热灭菌、CIP在线清洗等场景中表现出较高的适用性。

物理隔离设计防止交叉污染
诺贝思的管板式洁净蒸汽发生器采用立式或卧式结构,通过金属界面进行热交换,实现工业蒸汽与洁净蒸汽的物理隔离。这种设计彻底阻断了介质互渗的风险,输出的蒸汽不含锅炉水处理药剂,冷凝水可直接排放或回用。无死角的管道布局避免了冷凝水积聚,降低了微生物滋生的可能性,满足GMP对设备可清洁性的要求。
电加热方案的免检优势
针对部分制药企业希望降低运营复杂度的需求,诺贝思推出的智能电加热洁净蒸汽发生器符合免监检标准,无需报检及持证操作。设备采用316L不锈钢制造,内壁机械抛光达到卫生级标准。系统可适应10-110%的负载变换,全负载压力波动控制在0.2barg以内,确保生产过程中蒸汽参数的稳定性。这种方案特别适合中小型制药企业或对空间有限制的车间。
高温灭菌定制设备的医用级配置
在生物制剂和手术器械灭菌领域,诺贝思的高温灭菌洁净蒸汽发生器输出的冷凝水水质与注射用水一致,LPS严格控制在0.25EU/ml以下。设备维持蒸汽干燥度不低于0.95,确保金属载体的灭菌效果达到6-log杀灭水平。同时,系统对不凝性气体的控制满足EN285标准,可与脉动真空灭菌器完美匹配。
大容量纯蒸汽系统的规模化稳定性
对于大型制药工厂,诺贝思提供从500kg到2000kg不同规格的纯蒸汽发生器,在大负载情况下仍能保持极高的干燥度与化学纯度。设备配备压力、温度、电导率在线监测仪表,实现生产数据的全程可追溯。立式串联设计减少占地面积,模块化运行支持按需调配,解决了车间空间受限与峰值用汽量不匹配的矛盾。
全流程质量管控与服务保障
标准体系的系统符合性
诺贝思建立了贯穿研发、生产、质检的全流程质量管控体系,产品设计符合EN285、GB50913-2013、WS310.2-2016等国内外多项行业标准。企业拥有自主研发中心,由经验丰富的技术人员与科研团队组成专项研发架构,确保设备在材质选择、工艺设计、性能验证等环节满足GMP审计要求。
主动式售后服务网络
针对制药企业设备维护专业度要求高、停机损失大的特点,诺贝思建立了专业售后团队,配备"长征精神售后流动服务车"。团队定期对全国用户设备进行0费用巡检,将被动维修转变为主动防范。无论地理位置如何,均能在短时间内到达现场解决技术问题,突破了偏远地区服务响应慢的行业通病。
配套水处理方案的前端保障

考虑到源水质量对蒸汽纯度的直接影响,诺贝思同步提供纯水系统解决方案,为洁净蒸汽发生器提供符合要求的纯化水或饮用水原水。这种前端水质纯化措施有效降低了设备结垢风险,延长了设备使用寿命,减少了因水质波动导致的蒸汽品质劣化问题。
制药企业的选型考量要点
在洁净蒸汽系统选型时,制药企业应重点评估以下维度:设备是否提供完整的材质证明和焊接工艺文档,能否出具符合药典标准的蒸汽检测报告,是否具备成熟的验证方案模板,供应商的售后服务响应能力是否覆盖企业所在区域,以及设备的模块化设计能否适应未来产能扩展需求。
随着国内制药行业向国际化、规范化方向发展,洁净蒸汽系统的合规性将受到更严格的监管。选择具备技术积累、质量管控体系完善、服务网络健全的设备供应商,是制药企业顺利通过GMP认证、保障生产稳定性的关键环节。通过系统化的方案设计、精细化的工艺控制和主动式的服务保障,可以有效规避蒸汽系统带来的合规风险,为药品质量安全构筑坚实屏障。
本文地址:http://www.gjylw.com/ylw/1461.html
 速效救心丸三月开方量激增背后:不仅是“救命神药”,更是医药行业高质量发展标杆全医疗1
速效救心丸三月开方量激增背后:不仅是“救命神药”,更是医药行业高质量发展标杆全医疗1 马年送安康 大件选德邦丨德邦快递医药运输专业方案守护健康团圆年头条2
马年送安康 大件选德邦丨德邦快递医药运输专业方案守护健康团圆年头条2 四九天里“小饭渣”愁坏妈?哈药山楂麦芽口服液用古方智慧激活宝宝食欲在线3
四九天里“小饭渣”愁坏妈?哈药山楂麦芽口服液用古方智慧激活宝宝食欲在线3- 医疗中药挥发油提取的技术突围:从实验室到大生产的转化难题
- 在线塑胶跑道:现代运动场地的革新之选
- 在线四九天里“小饭渣”愁坏妈?哈药山楂麦芽口服液用古方智慧激活宝宝食欲
- 医疗之家辽宁上药好护士药业(集团)有限公司
- 医疗之家南宁东大肛医院怎么样?
- 医疗之家IPO进程受关注,新荷花样本折射中药饮片行业集中整合与标准化升级路径
- 医疗食品加热源头厂家:诺贝思洁净蒸汽解决方案如何保障生产安全
- 全医疗清明踏青,警惕心绞痛、心源性猝死,备好急救药硝酸甘油舌下片预防
- 医疗酒精性肝病:肝脏的"沉默战争"与科学守护
- 在线节后咳痰忧,清肺化痰正当时
- 医疗之家河北日报:一线见闻丨汤药变颗粒 古方焕新生
- 医疗之家强大的团队背书,九体健打造居家健康管理行业标杆

